|
Ein Massenpunkt oder ein Körper ist nur
dann im mechanischen Gleichgewicht, wenn er sich im gewählten Koordinatensytem
nicht mehr bewegt; wenn also alle zeitlichen Ableitungen relevanter Ortsgrößen
(z.B. Koordinaten des Schwerpunkts, Winkel) = Null sind. |
|
 |
Das ist dann, und nur dann der Fall, wenn
die Summe aller Kräfte und Drehmomente = Null ist. |
|
 |
Denn solange noch eine Kraft oder ein Drehmoment auf einen Körper wirkt, wird er sich
bewegen; er ist nicht im Gleichgewicht. |
|
 |
Der Einwand, daß man auf einen großen Stein eine kleine Kraft wirken lassen kann
ohne daß er sich bewegt, gilt nicht, denn in der klassischen Mechanik müssen
wir natürlich auch die Reibungskräfte oder die Reaktionskräfte der Unterlage mitzählen - und dann ist
die Summe der Kräfte wieder Null. |
 |
Da in den uns interessierenden Fällen (ohne mechanische Reibung, die es atomar
schlicht nicht gibt), die Kraft immer
durch die Ableitung des mechanischen Potentials, d. h. der potentiellen
Energie U(x,y,z) , gegeben ist, muß im mechanischen Gleichgewicht folgerichtig gelten
|
| |
Dreidimensional
¶U
¶x | = |
¶U
¶y |
= | ¶U
¶z | = | 0 |
|
|
 |
Das bedeutet, daß in einer Darstellung des Potentials über die Koordinaten
(x,y,z), oder, was gleichbedeutend ist, den Ortsvektor r, Gleichgewicht überall
dort vorliegt, wo U(r)
Extremwerte - Maxima oder Minima - hat. |
|
 |
Wenn man sich das mal aufmalt und kritisch anschaut, kann man noch einige
sinnvolle Fallunterscheidungen treffen. |
|
|
|
 |
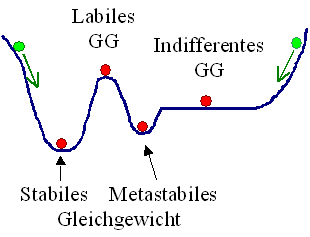
Auf ein Koordinatensystem wurde verzichtet, da dies eine ganz allgemeine Darstellung
sein soll. Die blaue Kurve kennzeichnet den Verlauf eines Potentials im Raum - ganz symbolisch und allgemein. |
|
 |
Und ein Potential ist eine Energie; dargestellt ist also in diesem allgemeinen
Fall eine Energie des Systems, hier ist es die potentielle
Energie. |
|
 |
Die beiden grünen Massenpunkte (oder, wenn wir die Darstellung symbolisch nehmen: Systeme), sind erkennbar nicht im Gleichgewicht; sie würden
sich in Pfeilrichtung bewegen. |
 |
Die roten Punkte sitzen an Stellen, an denen die Ableitung der Potentialkurve
= Null ist, d.h. per definitionem an Gleichgewichtspositionen. Wir können
aber noch verschiedene Gleichgewichtsarten unterscheiden, indem wir uns die Frage stellen,
was in einer gegeben Gleichgewichtsposition passieren würde, wenn man ein bißchen stört. |
|
 |
Im tiefsten Minimum, dem stabilen
Gleichgewicht, passiert im wesentlichen nichts. Eine Auslenkung des Systems in jede Richtung führt zu Kräften,
die das System in die GG-Lage (ab jetzt kürzen wir Gleichgewicht gelegentlich mit GG ab) zurücktreiben. Mit ein bißchen
Energiedissipation, d.h. Abgabe von Energie an andere Teilchen des Systems,
kommt das System wieder im stabilen GG zur Ruhe. |
|
 |
Das stabile mechanische
GG ist also gleichzeitig der Zustand mit der geringsten potentiellen Energie.
Unser System wird diesen Zustand anstreben; falls es in einem metastabilen Zustand "gefangen"
ist, hilft ein bißchen "Schütteln", d.h. Energiezufuhr; um es auf den Weg zu schicken. Das ist die
alte Aussage, daß Systeme zum Zustand geringstmöglicher
Energie streben; die wir aber in der weiteren Betrachtung relativieren müssen. |
|
 |
Dasselbe gilt zunächst im Nebenminum des metastabilen Gleichgewichts. Falls wir aber die Störung zu groß machen, läuft
uns das System davon ins stabile Gleichgewicht. Wir sehen auch, daß wir ein definiertes
Maß an Energie brauchen, um von einem metastabilen in ein stabiles Gleichgewicht zu kommen. Wir müssen mindestens soviel Energie zuführen, daß wir den linken Berg erklimmen können. |
|
 |
Zwischen den beiden Tälern liegt ein Maximum. Auch dort ist dU/dx =
0; es ist die Position des labilen Gleichgewichts. Bei der geringsten Störung
wird das System ins stabile oder metastabile GG umklappen. |
|
 |
In Bereichen, in denen das Potential überall konstant ist, ist dU/dx
überall = Null; bei jeder Position ist indifferentes Gleichgewicht
gegeben. Bei einer kleinen Störung (immer mit Energiedispersion gedacht), bleibt das System einfach in der neuen Position
stehen. |
 |
Wir erkennen sofort, daß diese Betrachtung komplett übertragbar ist
auf das elektrische Potential und die damit verbundene elektrostatische
Energie sowie auf eine Kombination beider Energien. Das elektrostatisches GG
ist also mit der Betrachtung des mechanischen Gleichgewichts gleich miterledigt. |
 |
Eine wichtige weitere Erkenntnis kann damit gewonnen werden: |
|
 |
Hat ein System das mechanische stabile Gleichgewicht erreicht, und ist es
von der Außenwelt abgeschlossen, wird sich nie wieder etwas ändern.
|
|
 |
Denn es sind keine Kräfte mehr da und es können
auch keine mehr auftreten (es ist kein Einfluß von außen erlaubt). |
 |
Wir verallgemeinern diese Erkennnis probeweise erst einmal und postulieren: |
|
 |
Gleichgewicht in einem System liegt dann vor, wenn sich
ohne Eingriff von außen nie wieder "etwas" ändert. Der Begriff
"Gleichgewicht" soll dabei auch Gleichgewichtsarten umfassen, die wir erst kennenlernen werden. |
 |
Systeme im Gleichgewicht sind quasi "tot";
und das Gleichgewicht ist das, was ein System anstrebt - darüber kann man mal ein bißchen nachdenken. |
 |
Betrachten wir nun nicht ein Massepünktchen oder ein durch einen Punkt symbolisiertes
System, sondern ein System mit vielen unabhängigen Massepunkten - ein Gas, eine
Flüssigkeit, einen Festkörper - dessen potentielle Energie überall konstant
ist, erhalten wir für das mechanische GG folgende Aussage: |
|
 |
Im mechanischen GG eines Systems von
Massepunkten in einem konstanten Potential liegt indifferentes
GG vor; als Konsequenz ist der Druck überall gleich groß. Schaun'
mer mal warum: |
|
 |
Bei einem Gas oder einer Flüßigkeit in einem nicht zu großen Volumen sind
die Massenpunkte - die Atome - überall "gleich gern", denn überall ist dU/dx = 0
(wenn man von dem im Vergleich zur kinetischen Energie sehr kleinen Höhenabhängigkeit der potentiellen Energie
mal absieht, die in einem nicht zu großen Volumen keine Rolle spielt). |
|
 |
Sofern die Teilchen sich bewegen können - bei Gasen und Flüssigkeiten also immer - werden sie dann den Raum mit konstanter Dichte
ausfüllen. |
|
 |
Ihre potentielle Energie ist - immer im Mittel - konstant,
die Gesamtenergie sowieso, also muß auch die kinetische Energie (im Mittel) konstant sein. |
 |
Wir haben hier gegenüber dem simplen Bild eines im GG ruhenden Massepunkt
eine erste Modifikation des Begriffes des mechanischen Gleichgewichts: Wír lassen für
das GG auch noch konstante mittlere kinetische Energien zu. |
|
 |
Wir beginnen also (zwangsweise) als wesentliche Parameter eines Systems vieler Teilchen irgendwelche
Mittelwerte anzuschauen; wir machen statistische Betrachtungen. |
|
 |
Zwangsweise deshalb, weil es weder möglich ist, den ca. 1023 Teilchen
in ein paar Liter Luft einzeln zu folgen, noch wäre es sinnvoll falls man es könnte. |
 |
Druck ist atomistisch nichts anderes, als die auf eine Gefäßwand ausgeübte Kraft.
|
|
 |
Diese Kraft kommt von der Impulsänderung der auf
die Gefäßwand aufprallenden Teilchen, und ist damit proportional ist zur Zahl der Teilchen (gegeben durch die
Dichte) die pro Zeiteinheit auf die Wand aufprallen und zu der mittleren kinetischen Energie der Teilchen.
|
|
 |
Sowohl Dichte als auch kinetische Energie sind aber konstant - damit ist auch der Druck konstant.
Und dies gilt für jede "Testfläche", die wir gedanklich irgendwo
im Behälter einbauen. |
 |
Bei großen Gasvolumina, bei denen das
Gravitationspotential "oben" und "unten" merklich verschieden ist - z.B. bei der Luftsäule über
unseren Köpfen - stimmt das natürlich nicht mehr: der Druck nimmt mit der
Höhe langsam ab. |
|
 |
Eine merkwürdige Frage kommt hoch: Wieso fallen die Luftmoleküle nicht alle "herunter"?
Auch das hat was mit Unordnung zu tun, wie wir später sehen werden. |
 |
Wie ist das nun bei Festkörpern, bei
Kristallen? Was bedeutet Druck in einem Kristall? |
|
 |
Schauen wir uns das Potential an: |
|
|
|
 |
Das Potential ist im oberen Teil der Zeichnung gezeigt, es ist periodisch.
Unsere Potentialtöpfe vom Kapitel 2.2 und Kapitel 2.3 überlagern sich, wie dort schon besprochen. |
|
 |
Die Atome üben durch Bindungen Kräfte auf ihre Nachbarn aus, können
also nicht ganz unabhängig voneinander in ihren Potentialtöpfen vibrieren. |
|
 |
Das kann man besser sehen, wenn man statt Potentialtöpfen symbolische "Federn"
zwischen den Atomen einführt wie im unteren Teil der Zeichnung gemacht. |
 |
Die Atome werden alle irgendwie um das Potentialminimum schwingen, d.h. kinetische
Energie besitzen, aber im Mittel sich alle im Potentialminimum aufhalten. |
|
 |
Die Kraft pro Fläche - das ist der Druck - den Atome
auf ihre Nachbarn ausüben, ist also im Gleichgewicht überall gleich groß;
wie oben behauptet. Denn nur dann können die Atome im Mittel im Potentialminimum sitzen.
|
|
 |
Unter Normalbedingungen (Atmosphärendruck), wird der Kristall solange zusammengedrückt
- die Bindungsabstände werden minimal kleiner - bis Druckausgleich erfolgt, d.h. im Kristallinnern der Druck gleichgroß
ist wie der äußere Druck. |
 |
Wir verschärfen damit die Aussage von oben noch etwas uind merken uns:
|
|
 |
Mechanisches Gleichgewicht in einem System vieler Teilchen ist gleichbedeutend
mit überall gleichem, d.h. konstantem Druck. |
 |
Mechanische Systeme in Ruhe sind aber zu einfach, um die Welt im Großen
zu verstehen. Wir müssen auf jeden Fall noch Bewegung mitnehmen, und das auch noch
bei Systemen die aus vielen Massenpunkten, d.h. aus Atomen oder Molekülen bestehen.
|
|
 |
Da wir aber nicht die individuellen Schicksale vieler Massepunkte verfolgen wollen (oder können),
müssen wir jetzt geeignete Mittelwerte einführen, die das Systen hinreichend
beschreiben. |
|
 |
Damit betrachten wir die Temperatur
eines Systems - wir müssen jetzt das thermische Gleichgewicht definieren und einführen. |
| |
| |
|
 |
Da Temperatur, wie wir wissen,
nur ein Maß für die mittlere ungeordnete kinetische Energie der Atome oder
Moleküle eines Gases, einer Flüßigkeit oder eines festen Körpers ist, heißt das, daß die
die mittlere Geschwindigkeit, mit der sich die Teilchen
in einem Gas oder einer Flüßigkeit bewegen (oder um eine Achse rotieren, oder in einem Festkörper um ihre
Gleichgewichtspositionen schwingen), überall (im Mittel) konstant
ist. |
|
 |
Das "ungeordnet" ist zwar trivial, aber wichtig.
Gibt man allen Atomen eines Körpers, z.B eines Autos, zusätzlich zu ihrer ungeordneten (Vibrations)bewegung noch
eine Geschwindigliet die für alle Atome nach Betrag und Richtung identisch ist, wird das Auto deswegen nicht heißer
- es fährt nur und steht nicht still. |
 |
Wir nehmen diese Aussage als Bedingung für das thermische
Gleichgewicht. Wie beim mechanischen Gleichgewicht interpretieren wir das thermische Gleichgewicht so, daß
es von sich selbst überlassenen Systemen immer angestrebt wird. |
|
 |
Diese Aussage folgt nicht direkt aus dem mechanischen Gleichgewicht. Es kann sehr wohl der
Druck überall konstant sein und die Temperatur ist verschieden, oder auch umgekehrt. |
 |
Wir schließen daraus: Sich selbst überlassene Systeme
streben mechanisches und thermisches Gleichgewicht an. |
 |
Wir nehmen nun das bisher Gelernte und wenden es auf ein Gas mit zwei
Teilchensorten an. |
|
 |
Nehmen wir an, wir haben H2 und O2 zusammengebracht
indem wir ein Ventil zwischen zwei Gasbehältern öffnen, die vor dem Öffnen den Druck pO
und pH sowie die Temperaturen TO und TH
hatten. Elektrische Felder sollen nicht vorliegen. |
|
 |
Es wird sich mechanisches und thermisches
Gleichgewicht einstellen, d.h. Druck und Temperatur werden sich ausgleichen und über kurz oder lang überall konstant
sein. |
|
 |
Aber ist dieser Zustand ein stabiles "globales"
Gleichgewicht im Sinne der früheren Definition? Gibt es jetzt keine Möglichkeit
mehr, daß sich irgendetwas ändert? |
 |
Aber ja doch! Ein bißchen
Energiezufuhr (eine kleine Störung) genügt um einen großen Knall auszulösen;
denn wir haben Knallgas hergestellt. |
|
 |
Eine Menge Energie geht "nach außen", die dem System jetzt fehlt - d.h. es
hat einen energetisch viel tieferen Platz gefunden; es konnte in einer geeigneten Potentialdarstellung
noch sehr viel tiefer sinken. |
 |
Denn es konnte noch eine chemische
Reaktion stattfinden; und erst nachdem aus Knallgas Wasser entstanden ist, wird sich nichts mehr ändern; erst
dann ist "globales" Gleichgewicht erreicht. |
|
 |
Wir müssen also eine weitere Gleichgewichtsart einführen, das chemische Gleichgewicht, um alle Änderungsmöglichkeiten unseres Systems abzudecken. |
|
 |
Der Begriff "chemisch" muß in diesem Zusammenhang
nicht stören; wir werden jetzt keine Chemie treiben. Der Begriff ist historisch entstanden, besser wäre eigentlich
der Ausdruck "Teilchenzahlengleichgewicht"; denn was sich ändert sind
die Zahlen der Teilchen - in unserem Beispiel der H2, O2 und H2O Moleküle.
|
|
 |
Aber auch wenn sich zum Beispiel die Zahl der Elektronen in einem mikroelektronischen Bauelement
ändert, ist das chemische Gleichgewicht gefragt - Elektronen sind Teilchen, und
es heißt nun mal so. |
|
 |
Wenn wir Wasser unter 0oC abkühlen, ändern sich auch
die Teilchenzahlen: Aus H2O Teilchen in der Dampfphase werden H2O
Teilchen in der Festphase - im Sinne der Gleichgewichtsthermodynamik sind das verschiedene Teilchen. |
 |
Das chemische Gleichgewicht ist also das wirklich interessante Gleichgewicht.
Denn der Weg eines Systems ins chemische Gleichgewicht enthält die nichtrivialen
Systemänderungen, die Möglichkeiten, über Änderungen von Teilchenzahlen die Eigenschaften
von Materialien zu beeinflussen. Es enthält weiterhin auch praktisch alle Materialänderungen, die man mit dem
Stichwort "Altern" beschreibt. |
|
 |
Grund genug, um sich das chemische Gleichgewicht im nächsten Kapitel genauer anzuschauen. |
| |
|
© H. Föll (MaWi 1 Skript)